Название: Сравнение изотермического реактора идеального вытеснения и реактора полного смешения в зависимости от степени превращения
Вид работы: контрольная работа
Рубрика: Химия
Размер файла: 88.31 Kb
Скачать файл: referat.me-368781.docx
Краткое описание работы: Основные параметры реакторов идеального вытеснения и полного смешения. Расчет необходимого времени пребывания реагентов в реакционной зоне. Параметры химико-технологического процесса в потоке полного смешения при изотермическом температурном режиме.
Сравнение изотермического реактора идеального вытеснения и реактора полного смешения в зависимости от степени превращения
Контрольная работа
Сравнение изотермического реактора идеального вытеснения и реактора полного смешения в зависимости от степени превращения
Введение
Серная кислота является одним из крупнотоннажных продуктов химической технологии. Серная кислота относиться к числу сильных кислот и является самой дешёвой. Она реагирует почти со всеми металлами, вступает в реакции обменного разложения. Почти половину всей вырабатываемой кислоты используют для производства минеральных удобрений. Также серную кислоту применяют в нефтехимической, металлургической отраслях промышленности, для производства химических волокон, красителей, взрывчатых веществ и других продуктов.
Окисление оксида серы (IV) является второй стадией производства cерной кислоты. По методу окисления оксида серы (IV) различают контактный и нитрозный способы производства серной кислоты. В современных производствах окисление проводят в присутствии твердого катализатора, и способ производства называют контактным. При нитрозном способе катализатором служат оксиды азота. Окисление проводят в жидкой фазе с помощью нитрозы, выполняющей функции передатчика кислорода.
Окисление оксида серы (IV) в оксид серы (VI) – основной процесс в производстве серной кислоты. Окисление проводят после тщательной очистки газа от пыли, тумана серной кислоты, контактных ядов и осушки.
Равновесие реакции окисления SO2 в соответствии с принципом Ле-Шателье сдвигается в сторону образования SO3 при понижении температуры и повышении давления. Равновесная степень превращения реагентов зависит также от соотношения SO2 и O2 в газе. Некаталитическое окисление оксида серы (IV) протекает столь медленно, что в производственных масштабах его проводить нецелесообразно. Поэтому процесс проводят в присутствии катализаторов. В сернокислой промышленности в разное время применяли лишь три вида катализаторов, основу которых составляли металлическая платина, оксиды железа и оксид ванадия (V). Самыми активными катализаторами являются платиновые. Однако из-за высокой чувствительности к контактным ядам, в частности к мышьяковистым соединениям, эти катализаторы уже давно не применяются.
Катализаторы на основе оксидов железа практически не отравляются, но достаточную активность он проявляет лишь при температуре выше 625С. При такой температуре равновесная степень превращения не превышает 70%, и использование таких катализаторов возможно лишь для так называемого предварительного окисления сернистого газа со степенью превращения 50-60%.
Ванадиевые катализаторы в условиях работы представляют собой пористый носитель, внутренняя поверхность которого смочена пленкой раствора V2 O5 в расплаве пиросульфата калия.
В рамках данной работы мы рассматриваем 2 типа реакторов: реактор идеального вытеснения и реактор полного смешения.
Реактор идеального вытеснения. При прохождении потока через данный реактор все частицы движутся с одной скоростью, не перемешиваясь друг с другом, то есть исходные реагенты не смешиваются с продуктами реакции. В каждом поперечном сечении потока концентрации их выровнены, но плавно изменяются по длине реакционной зоны. Аналогично изменяется скорость процесса.
По условию задания мы используем изотермический температурный режим, который характеризуется постоянством температуры по всей длине реакционной зоны. Данный режим в реакторе идеального вытеснения наблюдается в случае протекания химико-технологического процесса без теплового эффекта или когда скорость тепловыделения (теплопоглощения) мала, а теплопроводность среды в реакционной зоне высока.
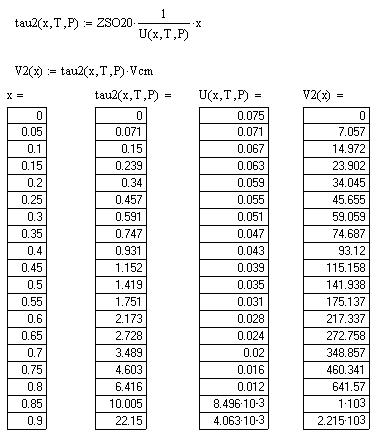
Необходимое время пребывания реагентов в реакционной зоне рассчитывают по уравнению:
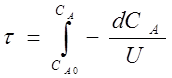 ,
,
называемому характеристическим уравнением реактора идеального вытеснения.
Реактор полного смешения. При прохождении потока через данный реактор частица, поступающая в реакционную зону, мгновенно смешиваются с частицами, уже находящимися в этой зоне, то есть равномерно распределяются по всей длине и во всем объёме зоны. В результате во всех точках реакционной зоны мгновенно выравниваются все параметры, характеризующие химико-технологический процесс.
Вследствие полного перемешивания выравнивается и температура во всём объёме реакционной зоны. Таким образом, химико-технологический процесс в потоке полного смешения может протекать только при изотермическом температурном режиме, независимо от значения теплового эффекта, концентрации и степени превращения исходных веществ.
Время пребывания частиц в реакционной зоне распределено не равномерно. Смешение исходных реагентов с продуктами реакции и неравномерность времени пребывания частиц в реакционной зоне приводит к уменьшению движущей силы процесса по сравнению с проведением его в потоке идеального вытеснения.
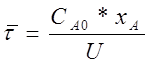 ,
,
это выражение называют характеристическим уравнением реактора полного смешения.
Целью данной работы является сравнение изотермического реактора идеального вытеснения и реактора полного смешения в зависимости от степени превращения, а также рассчитать производительность по исходному компоненту SO2 .
Исходные данные
SO2 + 0,5O2 = SO3 - ∆H0
![]()
Исходные концентрации реагентов (мольная доля):
![]()
Скорость реакции рассчитывается по выражению:
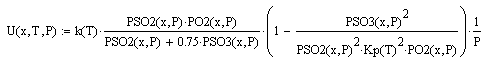
константа равновесия:
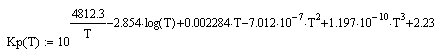
![]()
Расчетная часть
реактор идеальный вытеснение смешение

Вывод
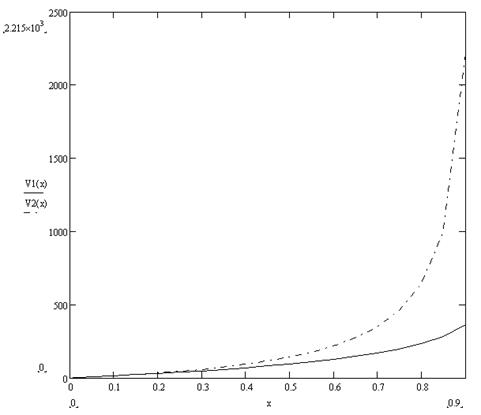
В результате проделанной работы мы выяснили, что объём реактора идеального вытеснения меньше объёма реактора полного смешения при одной и той же степени превращения, то есть при одинаковой скорости реакции.
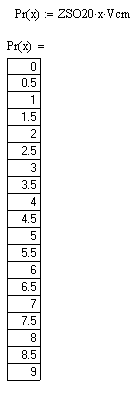
Производительность реакторов изменяется от 0 до 9 м3 /с с шагом 0,5 при соответственном изменении степени превращения SO2 от 0 до 0,9 с шагом 0,05.
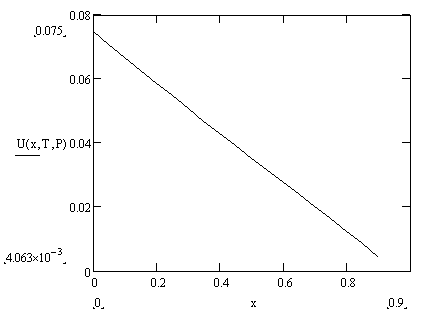
При увеличении степени превращения SO2 скорость реакции падает.
Похожие работы
-
Простейшие кинетические уравнения Кинетические кривые
Простейшие кинетические уравнения. Кинетические кривые. 3) Односторонняя реакция 2-го порядка и её стехиметрическое уравнение: Представим текущий материальный баланс для этой реакции в виде таблице:
-
Синтез циклогексанона
Расчет химического процесса синтеза циклогексанона: расходные коэффициенты, материальный и тепловой баланс. Термодинамический анализ основной реакции и константа равновесного состава реагирующих веществ. Расчет теплот сгорания и образования веществ.
-
Планирование дискриминирующих экспериментов
Эксперименты по дискриминации гипотез: химические, физико–химические, изотопные, кинетические. Идеальные реакторы для экспериментов: закрытый реактор полного смешения, проточный реактор идеального вытеснения. Критерии отсутствия диффузионного торможения.
-
Экспериментальные методы исследования гетерогенных катализаторов
Свойства и экспериментальное исследование гетерогенных катализаторов. Интегральные, дифференциальные лабораторные реакторы, их характеристика. Изотопные методы в катализе. Термопрограммированные десорбция и реакция. Физические основы флеш-десорбции.
-
Способы получения сложных эфиров. Конденсации формальдегида с изобутиленом. Различные способы получения фенола
Способы получения сложных эфиров. Основные продукты и области применения эфиров. Условия проведения реакции этерификации органических кислот со спиртами. Катализаторы процесса. Особенности технологического оформления реакционного узла этерификации.
-
Синтез химико-технологической схемы
Нахождение параметров уравнения Аррениуса методом наименьших квадратов. Получение статистической модели абсорбера с помощью метода Брандона. Математическое описание аппаратов. Синтез оптимальной тепловой системы с помощью эвристического метода.
-
Реакторы идеального вытеснения
Определение температуры газового потока на входе в реакторе, обеспечивающей максимальную производительность реактора. Программа для расчета, составляется в приложении REAC. График зависимости производительности реактора от температуры газового потока.
-
Основы химической технологии
Процесс произведения нитробензола и составление материального баланса нитратора. Определение расхода реагентов и объёма реактора идеального смешения непрерывного действия при проведении реакции второго порядка. Расчет теплового эффекта химической реакции.
-
Подготовка воды для производственных процессов. Изложение способов водоподготовки на предприятии
Промышленная водоподготовка. Комплекс операций, обеспечивающих очистку воды. Гомогенные и гетерогенные некаталитические процессы в жидкой и газовой фазах, их закономерности и способы интенсификации. Сравнение различных типов химических реакторов.
-
Выбор реактора для проведения реакции окисления сернистого ангидрида в серный ангидрид
Основные требования к промышленным реакторам. Термодинамика и кинетика окисления диоксида серы. Математические модели химических реакторов. Модель реактора идеального вытеснения и полного смешения. Получение максимальной степени окисления диоксида серы.