Название: Классификация аминокислот
Вид работы: статья
Рубрика: Биология и химия
Размер файла: 141.59 Kb
Скачать файл: referat.me-22246.docx
Краткое описание работы: Все встречающиеся в природе аминокислоты обладают общим свойством – амфотерностью (от греч. amphoteros – двусторонний), т.е. каждая аминокислота содержит как минимум одну кислотную и одну основную группы.
Классификация аминокислот
Березов Т.Т., Коровкин Б.Ф.
Все встречающиеся в природе аминокислоты обладают общим свойством – амфотерностью (от греч. amphoteros – двусторонний), т.е. каждая аминокислота содержит как минимум одну кислотную и одну основную группы. Общий тип строения α-аминокислот может быть представлен в следующем виде:

Как видно из общей формулы, аминокислоты будут отличаться друг от друга химической природой радикала R, представляющего группу атомов в молекуле аминокислоты, связанную с α-углеродным атомом и не участвующую в образовании пептидной связи при синтезе белка. Почти все α-амино- и α-карбоксильные группы участвуют в образовании пептидных связей белковой молекулы, теряя при этом свои специфические для свободных аминокислот кислотно-основные свойства. Поэтому все разнообразие особенностей структуры и функции белковых молекул связано с химической природой и физико-химическими свойствами радикалов аминокислот. Именно благодаря им белки наделены рядом уникальных функций, не свойственных другим биополимерам, и обладают химической индивидуальностью.
Классификация аминокислот разработана на основе химического строения радикалов, хотя были предложены и другие принципы. Различают ароматические и алифатические аминокислоты, а также аминокислоты, содержащие серу или гидроксильные группы. Часто классификация основана на природе заряда аминокислоты. Если радикал нейтральный (такие аминокислоты содержат только одну амино- и одну карбоксильную группы), то они называются нейтральными аминокислотами. Если аминокислота содержит избыток амино- или карбоксильных групп, то она называется соответственно основной или кислой аминокислотой.
Современная рациональная классификация аминокислот основана на полярности радикалов (R-групп), т.е. способности их к взаимодействию с водой при физиологических значениях рН (близких к рН 7,0). Различают 5 классов аминокислот, содержащих следующие радикалы: 1) неполярные (гидрофобные); 2) полярные (гидрофильные); 3) ароматические (большей частью неполярные); 4) отрицательно заряженные и 5) положительно заряженные. В представленной классификации аминокислот (табл. 1.3) приведены наименования, сокращенные английские и русские обозначения и однобуквенные символы аминокислот, принятые в отечественной и иностранной литературе, а также значения изоэлектрической точки (рI) и молекулярной массы (М). Отдельно даются структурные формулы всех 20 аминокислот белковой молекулы.


Полярные, незаряженные R-группы

Отрицательно заряженные R-группы

Положительно заряженные R-группы

Ароматические R-группы

Перечисленные аминокислоты присутствуют в разных количественных соотношениях и последовательностях в тысячах белков, хотя отдельные индивидуальные белки не содержат полного набора всех этих аминокислот. Помимо наличия в большинстве природных белков 20 аминокислот, в некоторых белках обнаружены производные аминокислот : оксипролин, оксилизин, дийодтирозин, фосфосерин и фосфотреонин (последние две аминокислоты представлены в главе 2):
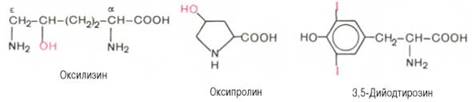
Первые две аминокислоты содержатся в белке соединительной ткани – коллагене, а дийодтирозин является основой структуры гормонов щитовидной железы. В мышечном белке миозине обнаружен также ε-N-метиллизин; в состав протромбина (белок свертывания крови) входит γ-карбоксиглутаминовая кислота, а в глутатионпероксидазе открыт селеноцистеин, в котором ОН-группа серина заменена на селен (Se):

Помимо указанных, ряд α-аминокислот выполняет важные функции в обмене веществ, хотя и не входит в состав белков, в частности орнитин, цитруллин, гомосерин, гомоцистеин, цистеинсульфиновая кислота, диоксифенилаланин и др.
Похожие работы
-
Виды аминокислот
Аминокислоты являются основными структурными единицами молекул белковых веществ. При гидролизе белков различной природы всегда получают смесь 20 аминокислот.
-
Влияние водных растворов аминокислот на пищевое поведение моллюска большого прудовика
Тип моллюски включает в себя животных, для которых новым сенсорным кана-лом, определяющим различные формы поведения, является хеморецепция.
-
Методы определения С-концевой аминокислоты
Для определения природы С-концевой аминокислоты часто используют ферментативные методы. Обработка полипептида карбоксипептидазой, которая разрывает пептидную связь с того конца пептида, где содержится свободная СООН-группа.
-
Методы определения N-концевой аминокислоты
Для определения природы N-концевой аминокислоты предложен ряд методов, в частности метод Сэнджера (F. Sanger), основанный на реакции арилирования полипептида 2,4-динитрофторбензолом (ДНФБ).
-
Общие свойства аминокислот
Кислотно-основные свойства. Эти свойства аминокислот определяют многие физико-химические и биологические свойства белков. На этих свойствах основаны, кроме того, почти все методы выделения и идентификации аминокислот.
-
Биосинтез белков
Основные формы связи аминокислот в молекулах белков. Способы синтеза белков в биологических организмах.
-
Нуклеиновые кислоты
Это высокомолекулярные биополимеры. Впервые были обнаружены в ядре в конце 19в., хотя они есть и в цитоплазме. Они состоят из мономеров, сложных химических соединений, - нуклеотид.
-
Эволюционная классификация
Подобно эмпирическим схемам классификации, эволюционная классификация основана на простом факте, что в природе встречаются ясно отличающиеся друг от друга группы, такие, как птицы, пингвины, летучие мыши, жуки и т. п.
-
Белки
Белки состоят из мономеров – аминокислот. Каждая аминокислота имеет аминогруппу, связанную с атомом углерода, с этим же атомом связана карбоксильная группа, водород и аминокислотный остаток. Такая конфигурация присутствует во всех аминокислотах.
-
Белки
Это линейные биополимеры состоящие из периодических мономеров (альфа аминокислот). Все 10 000 белков образованы 20 аминокислотами.