Название: Расчёт горения газового топлива. Определение состава и количества продуктов горения
Вид работы: лабораторная работа
Рубрика: Физика
Размер файла: 140.6 Kb
Скачать файл: referat.me-340406.docx
Краткое описание работы: Самарский Государственный Технический Университет Кафедра: «металловедение и порошковая металлургия» Лабораторная работа № 1 Расчёт горения газового топлива. Определение состава и количества продуктов горения.
Расчёт горения газового топлива. Определение состава и количества продуктов горения
Самарский Государственный Технический Университет
Кафедра: «металловедение и порошковая металлургия»
Лабораторная работа № 1
Расчёт горения газового топлива. Определение состава и количества продуктов горения.
Выполнил: студент III – ФТ - 1
Соловьева Ю.Б.
Проверил:
Якубович Е.А.
Самара 2009 г.
Цель работы – изучить методы и освоить практические навыки расчётов горения топлива на примере сжигания смеси газов.
Основные понятия и определения:
1) Теплота сгорания топлива
2) Количество необходимого для горения окислителя
3) Теоретическая и калориметрическая температура горения
4) Энтальпия
1) Теплота сгорания топлива:
![]() - для метана (полная реакция горения)
- для метана (полная реакция горения)
![]() - (не полная реакция горения)
- (не полная реакция горения)
При горении топлива, выделяется большое количество тепла. Как видно из реакции в продуктах сгорания присутствуют пары воды. В зависимости от того, в каком виде водяной пар находится в дымовых газах, различают высшую и низшую теплоту сгорания топлива.
Высшая теплота сгорания ( ![]() )
соответствует условию, при котором продукты горения охлаждаются до
)
соответствует условию, при котором продукты горения охлаждаются до ![]() (293 К), а пары воды конденсируются и охлаждаются до
(293 К), а пары воды конденсируются и охлаждаются до ![]() . При этом выделяется две составляющие тепла: теплота нагрева с 293 К до 373 К (418 кДж/кг),а также скрытая теплота парообразования испарения 2256,8 кДж/кг. Итого выделяется 2675,5 кДж/кг.
. При этом выделяется две составляющие тепла: теплота нагрева с 293 К до 373 К (418 кДж/кг),а также скрытая теплота парообразования испарения 2256,8 кДж/кг. Итого выделяется 2675,5 кДж/кг.
Низшая теплота сгорания (![]() )
соответствует условию, при котором содержащаяся в продуктах сгорания влага в виде пара охлаждается до температуры
)
соответствует условию, при котором содержащаяся в продуктах сгорания влага в виде пара охлаждается до температуры ![]() и не конденсируется. При этом выделяется:
и не конденсируется. При этом выделяется:
![]() ,
,
![]()
![]()
На практике в реальных условиях к сожалению, выделяется только низшая теплота сгорания.
2) Количество необходимого для горения окислителя (воздуха):
Количество окислителя определяется по уравнению реакции горения. Определённое количество является теоретическим. Для реального сжигания всегда подают несколько большее количество окислителя, т.к. есть потери . На 10 – 20 % больше.
Коэффициент избытка воздуха: ![]()
![]() - реальный объём,
- реальный объём, ![]() - теоретический объём.
- теоретический объём.
3) Температура горения: теоретическая и калориметрическая :
Необходимость введения двух определений связано с двумя возможными подходами процесса горения. А именно, с учётом или игнорированием затрат тепла на диссоциацию продуктов сгорания. Соответственно различают: теоретическую и калориметрическую температуру горения топлива:
![]()
![]()
![]() - теплота диссоциации.
- теплота диссоциации.
![]()
![]()
4) Энтальпия :
Это понятие является одним из фундаментальных в теплотехнике и термодинамике. По определению энтальпия представляет из себя произведение теплоёмкости на температуру:
![]()
Практическая часть
Рассмотрим горение газа состоящего из: 1) 93,48% метана (![]() ); 2) 3,85% этана (
); 2) 3,85% этана (![]() ); 3) 0,67% пропана (
); 3) 0,67% пропана (![]() ); 4) 0,3% бутана (
); 4) 0,3% бутана (![]() ); 0,75% углекислого газа (СО2) и 0,95% азота (
); 0,75% углекислого газа (СО2) и 0,95% азота (![]() ). Найти объём сгорания количества кислорода,
). Найти объём сгорания количества кислорода, ![]() и
и ![]() .
.
I . Определение необходимого количества воздуха:
1) ![]()
Из реакции видно, что для горения 1 моля ![]() нужно 2 моля
нужно 2 моля ![]() . 1 моль любого газа занимает 22,4
. 1 моль любого газа занимает 22,4 ![]() , это значит, что для сжигания 1
, это значит, что для сжигания 1![]() метана, нужно 2
метана, нужно 2![]()
![]() .
.
![]()
Известно, что в сухом воздухе содержится 21% ![]() , а остальное азот (
, а остальное азот (![]() ), 79%.
), 79%.
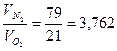
![]() .
.
2) ![]() - для этана;
- для этана;
![]()
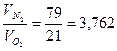
![]() .
.
3) ![]() - для пропана;
- для пропана;
![]()
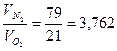
![]() .
.
4) ![]() - для бутана;
- для бутана;
![]()
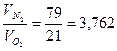
![]() .
.
Поскольку, реальное топливо – это смесь горючих газов, то общий расход воздуха определяется суммированием для отдельно горючих компонентов.
![]() .
.
II . Определение состава и количества продуктов сгорания:
Состав продуктов сгорания: ![]()
В состав объёма азота войдёт также азот из окислителя (воздуха).
1) для метана:
![]() ;
; ![]() ;
; ![]() .
.
![]() - суммарный объём продуктов сгорания.
- суммарный объём продуктов сгорания.
![]() =9,48%,
=9,48%, ![]() =18,81%,
=18,81%, ![]() =71,72%;
=71,72%;
2) для этана:
![]() ;
; ![]() ;
; ![]() .
.
![]() - суммарный объём продуктов сгорания.
- суммарный объём продуктов сгорания.
![]() =44,4%,
=44,4%, ![]() =10,57%,
=10,57%, ![]() =45,03%;
=45,03%;
3)для пропана:
![]() ,
, ![]() ,
, ![]() .
.
![]() - суммарный объём продуктов сгорания.
- суммарный объём продуктов сгорания.
![]() =16,75%,
=16,75%, ![]() =16,27%,
=16,27%, ![]() =66,98%;
=66,98%;
4) для бутана:
![]() ,
, ![]() ,
, ![]() .
.
![]() - суммарный объём продуктов сгорания.
- суммарный объём продуктов сгорания.
![]() =19,42%,
=19,42%, ![]() =14,94%,
=14,94%, ![]() =65,64%;
=65,64%;
Суммируем объёмы продуктов сгорания 4-х газов:
![]() ;
;
![]() ,
, ![]() ,
, ![]()
![]() =10,33%,
=10,33%, ![]() =18,59%,
=18,59%, ![]() =71,08%.
=71,08%.
III . Определение калориметрической и теоретической температуры:
Как видно, для расчёта калориметрической температуры нужно знать ![]() ,
, ![]() ,
, ![]() .
.
Требуемую для расчёта ![]() находят расчётным путём, зная тепловые эффекты реакции горения (таблица) и входящие в состав топлива доли соединений.
находят расчётным путём, зная тепловые эффекты реакции горения (таблица) и входящие в состав топлива доли соединений.
![]() ; (
; (![]() );
);
![]() .
.
Для определения температуры ,воспользуемся понятием энтальпии и определим энтальпию продуктов сгорания ![]() :
:
![]() ;
; ![]() ;
;
С другой стороны, ![]() есть сумма энтальпий конкретно составляющих продукты сгорания:
есть сумма энтальпий конкретно составляющих продукты сгорания: ![]()
Зададимся возможной температурой продуктов сгорания ![]() и найдём энтальпию продуктов сгорания при этой температуре:
и найдём энтальпию продуктов сгорания при этой температуре:
![]() ;
;
![]() ;
;
![]() ;
;
Если величина ![]() ,
то значит нами принята низкая температура в
,
то значит нами принята низкая температура в ![]() ,
тогда находим величину энтальпии для большей температуры на
,
тогда находим величину энтальпии для большей температуры на ![]() ,
т.е. для
,
т.е. для ![]() :
:
![]() ;
;
![]() ;
;
![]() ;
;
![]() ;
;
Обычно, ![]() ,
в этом случае, считается, что действительная калориметрическая температура лежит в пределах
,
в этом случае, считается, что действительная калориметрическая температура лежит в пределах ![]() и конкретное её значение находится методом интерполяции по формуле:
и конкретное её значение находится методом интерполяции по формуле:
![]() ;
;
![]() .
.
![]()
![]() .
.
Вывод: вычислили расход воздуха:
![]() ,
, ![]() ,
, ![]()
![]() =10,33%,
=10,33%, ![]() =18,59%,
=18,59%, ![]() =71,08%.
=71,08%.
количество продуктов сгорания:
![]()
определили температуру калориметрическую и теоретическую:
![]() ;
;
![]() .
.
Похожие работы
-
Теория горения
Физико-химические основы горения, его основные виды. Характеристика взрывов как освобождения большого количества энергии в ограниченном объеме за короткий промежуток времени, его типы и причины. Источники энергии химических, ядерных и тепловых взрывов.
-
Топливо и расчеты процессов горения
ФЕДЕРАЛЬНОЕ АГЕНТСТВО ПО ОБРАЗОВАНИЮ ГОУ ВПО Тюменский государственный архитектурно-строительный университет Кафедра «Промышленной теплоэнергетики»
-
Строение атома. Оптические спектры атома
Экспериментальное наблюдение характеристического излучения атома натрия в возбуждённом состоянии - в процессе горения; определение длины волны и энергетического уровня перехода наружного электрона, которым обусловлен характеристический цвет излучения.
-
Изучение скорости горения высокоэнергетических смесевых твердых топлив
Определение зависимости скорости горения баллистических и смесевых порохов от давления, химической структуры взрывчатых веществ. Анализ влияния положительных и отрицательных катализаторов на горение индивидуальных взрывчатых веществ различных классов.
-
Конвективный теплообмен
Основные понятия конвективного теплообмена: конвекция, коэффициент теплоотдачи, термическое сопротивление теплоотдачи, сущность процессов теплообмена. Циклонные топки для сжигания дробленого угля. Характеристики газообразного топлива, доменного газа.
-
Расчет барабанной сушильной установки
Этапы разработки сушильной установки: расчет энтальпии и влагосодержания продуктов сгорания топлива, расхода (суммарного, полезного, удельного) теплоты, коэффициента теплоотдачи, средней скорости сушильного агента и степени заполнения барабана песком.
-
Расчёт металлургической печи
В работе рассчитывается металлургическая печь с двусторонним обогревом, предназначенная для нагрева изделий из углеродистой стали. Определение коэффициетов теплоотдачи продуктов сгорания. Расчет горения топлива, нагрева металла, основных размеров печи.
-
Тепловой баланс котла по упрощенной методике теплотехнических расчетов
Расчет объемов воздуха, продуктов горения, жаропроизводительности топлива с учетом влаги в воздухе. Составление теплового баланса котлоагрегата по упрощенной методике теплотехнических расчетов Равича. Определение коэффициента полезного действия котла.
-
Газотурбинный двигатель 2
Газотурбинный двигатель Газотурбинный двигатель (ГТД), тепловой двигатель, в котором газ сжимается и нагревается, а затем энергия сжатого и нагретого газа преобразуется в механическую работу на валу газовой турбины. Рабочий процесс ГТД может осуществляться с непрерывным сгоранием топлива при постоянном давлении или с прерывистым сгоранием топлива при постоянном объёме.
-
Расчет процесса горения газообразного топлива
Расчет теоретического объёма расхода воздуха, необходимого для горения природного газа и расчет реального объёма сгорания, а также расчет теоретического и реального объёма продуктов сгорания. Сопоставление расчетов, используя коэффициент избытка воздуха.