Название: Электрохимическая коррозия с водородной деполяризацией
Вид работы: отчет по практике
Рубрика: Физика
Размер файла: 52.39 Kb
Скачать файл: referat.me-343528.docx
Краткое описание работы: Федеральное агентство по образованию РФ Южно-Уральский государственный университет Кафедра «Физическая химия» Дисциплина ________________________________________________________
Электрохимическая коррозия с водородной деполяризацией
Федеральное агентство по образованию РФ
Южно-Уральский государственный университет
Кафедра «Физическая химия»
Дисциплина ________________________________________________________
О Т Ч Е Т
по лабораторной работе
«Электрохимическая коррозия с водородной деполяризацией»
Студент группы_______________
____________________________
Челябинск
![]()
Цель работы : установить зависимость скорости коррозии железоуглеродистых сплавов в разбавленной серной кислоте от содержания углерода в сплаве.
Общие положения
В разбавленном растворе серной кислоты (до 20 мас.% H2 SO4 , р Н » 1) железоуглеродистые сплавы корродируют с водородной деполяризацией:
катодный процесс: 2 H+
(
p-
p)
+ 2 ![]() ® Н2 (газ)
|´1 (1)
® Н2 (газ)
|´1 (1)
анодный процесс: Fe(тв)
- 2 ![]() ®Fe2+
(р-р)
|´1 (2)
®Fe2+
(р-р)
|´1 (2)
суммарное уравнение: H2 SO4 ( p- p) + Fe(тв) ® Н2 (газ) + FeSO4 ( p- p) (3)
Водородная деполяризация протекает в кинетическом режиме (самая медленная стадия – или разряд ионов водорода, или рекомбинация атомов водорода в молекулу). Пузырьки водорода формируются преимущественно на поверхности катодных структурных составляющих сплавов (в сталях – на цементите, в сером чугуне – на графите). Поэтому возрастание скорости коррозии uкорр
при постоянной температуре возможно за счет экстенсивного фактора – увеличения площади S
К
катодных участков (при этом скорость ![]() коррозии на единице площади поверхности не изменяется):
коррозии на единице площади поверхности не изменяется):
![]() . (4)
. (4)
Площадь катодных участков на поверхности сплава пропорциональна концентрации углерода в сплаве, поэтому существует зависимость – чем больше содержание углерода, тем больше скорость коррозии сплава.
С ростом температуры скорость химической реакции возрастает в соответствии с уравнением Аррениуса. Для процесса водородной деполяризации это проявляется в уменьшении поляризации катодного процесса. Установлено, что при увеличении температуры на 1 градус перенапряжение выделения водорода уменьшается, в среднем, на 2 мВ. Поэтому с увеличением температуры скорость коррозии железоуглеродистых сплавов в кислых растворах резко возрастает.
Обработка результатов
Таблица 1 – Исходные данные образцов
| Марка сплава | 08КП | Ст3 | 45 | У10 | АЧС-3 |
| Содержание углерода С, мас.% | 0,09 | 0,24 | 0,43 | 0,96 | 3,5 |
| Плотность материала r, г/см3 | 7,85 | 7,7 | 7,7 | 7,6 | 7,1 |
| Диаметр образца d , мм | |||||
| Толщина образца h , мм | |||||
Площадь поверхности образца, см2 : S = 2×(p×d 2 /4) + p×d ×h |
Таблица 2 – Экспериментальные результаты
| Время t, мин |
Объем водорода (абсолютное значение и на единицу площади образца) | |||||||||
| 08КП | Ст3 | 45 | У10 | АЧС-3 | ||||||
| u, см3 |
u/S
, см3 /см2 |
u, см3 |
u/S
, см3 /см2 |
u, см3 |
u/S
, см3 /см2 |
u, см3 |
u/S
, см3 /см2 |
u, см3 |
u/S
, см3 /см2 |
|
| 0 | ||||||||||
|
1. Строим графики зависимости объема выделившегося водорода от длительности коррозии u/S = f (t) для каждого сплава (вместе 08КП, Ст3 и 45; вместе У10 и АЧС-3):
|
|
2. Скорость коррозии u/(S ×t) вычисляем как угловой коэффициент наклона линейной зависимости u/S = f (t). Для этого выбираем на линии графика две точки и по их координатам вычисляем угловой коэффициент наклона:
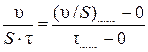 . (5)
. (5)
3. Объемный показатель коррозии вычисляем по формуле
![]() , (6)
, (6)
где Р = …….…..……. , мм.рт.ст. - фактическое атмосферное давление; Т = ……..……… , К - температура. В формуле учтены: переход от минут к часам; пересчет объема водорода к нормальным условия (давление 760 мм.рт.ст., температура 273 К).
3. Массовый показатель коррозии железа К m вычисляем из объемного показателя коррозии К об на основе эквивалентного соотношения между массой прореагировавшего железа и объемом выделившегося водорода (см. уравнение химической реакции (3)):
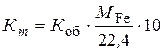 . (8)
. (8)
4. Глубинный показатель коррозии (проницаемость):
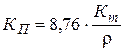 . (7)
. (7)
Таблица 3 – Результаты расчета показателей коррозии
| Марка сплава | 08КП | Ст3 | 45 | У10 | АЧС-3 |
| Скорость коррозии u/(S ×t), см3 /(см2 ×мин) |
|||||
| Объемный показатель коррозии К об , см3 /(см2 ×час) |
|||||
| Массовый показатель коррозии К m , г/(м2 ×час) |
|||||
| Глубинный показатель коррозии (проницаемость) КП , мм/год |
5. Строим график зависимости массового показателя коррозии К m от концентрации углерода в сплаве:
Таблица 4 – Десятибалльная шкала
|
|
4. Оцениваем стойкость железоуглеродистых сплавов в соответствии со шкалой коррозионной стойкости (табл. 4):
| Марка сплава | № группы | Название группы стойкости | Балл |
| 08КП | |||
| Ст3 | |||
| 45 | |||
| У10 | |||
| АЧС-3 |
ВЫВОД:
Вариант 1 «Электрохимическая коррозия с водородной деполяризацией»
| Марка сплава | 08КП | Ст3 | 45 | У10 | АЧС-3 |
| Толщина образца h , мм | 1,3 | 2,2 | 2,1 | 3,0 | 1,7 |
| Диаметр образца d , мм | 9,0 | 15,0 | 12,6 | 10,0 | 8,0 |
Объем водорода, см3
| Время, мин | 08КП | Ст3 | 45 | У10 | АЧС-3 |
| 0 | 0 | 0 | 0 | 0 | 0 |
| 5 | 0,1 | 0,3 | 0,4 | 1,4 | 11,8 |
| 10 | 0,1 | 0,5 | 0,8 | 3,3 | 22,6 |
| 15 | 0,2 | 0,8 | 1,3 | 4,9 | 35,0 |
| 30 | 0,2 | 1,5 | 2,8 | 11,0 | 66,6 |
| 45 | 0,3 | 2,3 | 4,6 | 16,3 | 95,4 |
| 60 | 0,4 | 3,2 | 6,2 | 23,0 |
Вариант 2 «Электрохимическая коррозия с водородной деполяризацией»
| Марка сплава | 08КП | Ст3 | 45 | У10 | АЧС-3 |
| Толщина образца h , мм | 1,8 | 1,8 | 1,8 | 1,8 | 1,8 |
| Диаметр образца d , мм | 10 | 14 | 12 | 12 | 10 |
Объем водорода, см3
| Время, мин | 08КП | Ст3 | 45 | У10 | АЧС-3 |
| 0 | 0 | 0 | 0 | 0 | 0 |
| 5 | 0,1 | 0,2 | 0,3 | 1,6 | 17,6 |
| 10 | 0,1 | 0,4 | 0,7 | 3,8 | 33,7 |
| 15 | 0,2 | 0,7 | 1,1 | 5,7 | 52,3 |
| 30 | 0,3 | 1,3 | 2,5 | 12,8 | 99,4 |
| 45 | 0,3 | 1,9 | 4,0 | 19,0 | |
| 60 | 0,5 | 2,7 | 5,5 | 26,8 |
Вариант 3 «Электрохимическая коррозия с водородной деполяризацией»
| Марка сплава | 08КП | Ст3 | 45 | У10 | АЧС-3 |
| Толщина образца h , мм | 2 | 2 | 2 | 2 | 2 |
| Диаметр образца d , мм | 10 | 12 | 13 | 14 | 8 |
Объем водорода, см3
| Время, мин | 08КП | Ст3 | 45 | У10 | АЧС-3 |
| 0 | 0 | 0 | 0 | 0 | 0 |
| 5 | 0,1 | 0,2 | 0,4 | 2,2 | 12,4 |
| 10 | 0,1 | 0,3 | 0,8 | 5,2 | 23,8 |
| 15 | 0,3 | 0,5 | 1,3 | 7,7 | 36,9 |
| 30 | 0,3 | 1,0 | 2,9 | 17,3 | 70,2 |
| 45 | 0,4 | 1,5 | 4,8 | 25,6 | 99,85 |
| 60 | 0,5 | 2,1 | 6,5 | 36,1 | – |
Вариант 1 «Электрохимическая коррозия с водородной деполяризацией»
| Марка сплава | 08КП | Ст3 | 45 | У10 | АЧС-3 |
| Толщина образца h , мм | 1,3 | 2,2 | 2,1 | 3,0 | 1,7 |
| Диаметр образца d , мм | 9,0 | 15,0 | 12,6 | 10,0 | 8,0 |
Объем водорода, см3
| Время, мин | 08КП | Ст3 | 45 | У10 | АЧС-3 |
| 0 | 0 | 0 | 0 | 0 | 0 |
| 5 | 0,1 | 0,3 | 0,4 | 1,4 | 11,8 |
| 10 | 0,1 | 0,5 | 0,8 | 3,3 | 22,6 |
| 15 | 0,2 | 0,8 | 1,3 | 4,9 | 35,0 |
| 30 | 0,2 | 1,5 | 2,8 | 11,0 | 66,6 |
| 45 | 0,3 | 2,3 | 4,6 | 16,3 | 95,4 |
| 60 | 0,4 | 3,2 | 6,2 | 23,0 |
Вариант 2 «Электрохимическая коррозия с водородной деполяризацией»
| Марка сплава | 08КП | Ст3 | 45 | У10 | АЧС-3 |
| Толщина образца h , мм | 1,8 | 1,8 | 1,8 | 1,8 | 1,8 |
| Диаметр образца d , мм | 10 | 14 | 12 | 12 | 10 |
Объем водорода, см3
| Время, мин | 08КП | Ст3 | 45 | У10 | АЧС-3 |
| 0 | 0 | 0 | 0 | 0 | 0 |
| 5 | 0,1 | 0,2 | 0,3 | 1,6 | 17,6 |
| 10 | 0,1 | 0,4 | 0,7 | 3,8 | 33,7 |
| 15 | 0,2 | 0,7 | 1,1 | 5,7 | 52,3 |
| 30 | 0,3 | 1,3 | 2,5 | 12,8 | 99,4 |
| 45 | 0,3 | 1,9 | 4,0 | 19,0 | |
| 60 | 0,5 | 2,7 | 5,5 | 26,8 |
Вариант 3 «Электрохимическая коррозия с водородной деполяризацией»
| Марка сплава | 08КП | Ст3 | 45 | У10 | АЧС-3 |
| Толщина образца h , мм | 2 | 2 | 2 | 2 | 2 |
| Диаметр образца d , мм | 10 | 12 | 13 | 14 | 8 |
Объем водорода, см3
| Время, мин | 08КП | Ст3 | 45 | У10 | АЧС-3 |
| 0 | 0 | 0 | 0 | 0 | 0 |
| 5 | 0,1 | 0,2 | 0,4 | 2,2 | 12,4 |
| 10 | 0,1 | 0,3 | 0,8 | 5,2 | 23,8 |
| 15 | 0,3 | 0,5 | 1,3 | 7,7 | 36,9 |
| 30 | 0,3 | 1,0 | 2,9 | 17,3 | 70,2 |
| 45 | 0,4 | 1,5 | 4,8 | 25,6 | 99,85 |
| 60 | 0,5 | 2,1 | 6,5 | 36,1 | – |
Похожие работы
-
Топливо и расчеты процессов горения
ФЕДЕРАЛЬНОЕ АГЕНТСТВО ПО ОБРАЗОВАНИЮ ГОУ ВПО Тюменский государственный архитектурно-строительный университет Кафедра «Промышленной теплоэнергетики»
-
Исследование автогенератора с частной модуляцией
ФЕДЕРАЛЬНОЕ АГЕНТСТВО ПО ОБРАЗОВАНИЮ ГОСУДАРСТВЕННОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ ВЫСШЕГО ПРОФЕССИОНАЛЬНОГО ОБРАЗОВАНИЯ ВЯТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ
-
Изучение прямолинейного движения тел на машине Атвуда 3
Федеральное Агентство по образованию ТОМСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ СИСТЕМ УПРАВЛЕНИЯ И РАДИОЭЛЕКТРОНИКИ (ТУСУР) Кафедра физики ОТЧЕТ Лабораторная работа по курсу "Общая физика"
-
Электроматериалы
ФЕДЕРАЛЬНОЕ АГЕНТСТВО ПО ОБРАЗОВАНИЮ __________________________________________________________________ГОСУДАРСТВЕННОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ
-
Закон Ома 2
Федеральное агентство по образованию Ухтинский государственный технический университет Кафедра электрификации и автоматизации технологических процессов
-
Исследование однофазного транзисторного преобразователя с широтно-импульсной модуляцией
Федеральное Агентство по Образованию РФ ТОМСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ СИСТЕМ УПРАВЛЕНИЯ И РАДИОЭЛЕКТРОНИКИ (ТУСУР) Кафедра ПрЭ Лабораторная работа №1
-
Исследование цепей постоянного тока
Преобразование источника тока в эквивалентный ему источник. Расчет собственного сопротивления контуров и сопротивления, находящиеся на границе. Расчет методом узловых потенциалов. Составление расширенной матрицы, состоящей из проводимостей и токов.
-
Расчет цепей постоянного тока
Определение всех неизвестных токов и сопротивления, величины и полярности с помощью законов Кирхгофа и Ома. Электрическая схема, получающаяся при замыкании ключей. Расчет схемы с двумя узлами методом узлового напряжения. Уравнение баланса мощностей.
-
Расчет электрических цепей постоянного тока
Федеральное агентство по образованию Федеральное государственное образовательное учреждение Высшего профессионального образования «СИБИРСКИЙ ФЕДЕРАЛЬНЫЙ УНИВЕРСИТЕТ»
-
Термодинамический анализ цикла газовой машины
Газовый цикл и его четыре процесса, определяемые по показателю политропы. Параметры для основных точек цикла, расчет промежуточных точек. Расчет постоянной теплоемкости газа. Процесс политропный, изохорный, адиабатный, изохорный. Молярная масса газа.


