Название: Химическая кинетика и равновесие
Вид работы: реферат
Рубрика: Химия
Размер файла: 180.11 Kb
Скачать файл: referat.me-368848.docx
Краткое описание работы: Химическая кинетика Химическое равновесие Химическая кинетика – раздел химии, который изучает скорость химической реакции и факторы влияющие на неё.
Химическая кинетика и равновесие
Химическая кинетика
Химическое равновесие
Химическая кинетика – раздел химии, который изучает скорость химической реакции и факторы влияющие на неё.
О принципиальной осуществимости процесса судят по значению изменения энергии Гиббса системы. Однако оно ничего не говорит о реальной возможности реакции в данных условиях, не даёт представления о скорости и механизме процесса.
Изучение скоростей реакций позволяет выяснить механизм сложных химических превращений. Это создаёт перспективу для управления химическим процессом, позволяет осуществлять математическое моделирование процессов.
Реакции могут быть:
1. гомогенными – протекают в одной среде (в газовой фазе); проходят во всём объёме;
2. гетерогенными – протекают не в одной среде (между веществами, находящимися в разных фазах); проходят на границе раздела.
Под скоростью химической реакции понимают число элементарных актов реакции, проходящих в единицу времени в единице объёма (для гомогенных реакций) и на единицу поверхности (для гетерогенных реакций).
Так как при реакции изменяется концентрация реагирующих веществ, то скорость обычно определяют как изменение концентрации реагентов в единицу времени и выражают в ![]() . При этом нет необходимости следить за изменением концентрации всех веществ, входящих в реакцию, поскольку стехиометрический коэффициент в уравнении реакции устанавливает соотношение между концентрациями, т.е. при
. При этом нет необходимости следить за изменением концентрации всех веществ, входящих в реакцию, поскольку стехиометрический коэффициент в уравнении реакции устанавливает соотношение между концентрациями, т.е. при ![]() скорость накопления аммиака вдвое больше скорости расходования водорода.
скорость накопления аммиака вдвое больше скорости расходования водорода.

![]()
![]() ,
, ![]() , т.к.
, т.к. ![]() не может быть отрицательной, поэтому ставят «–».
не может быть отрицательной, поэтому ставят «–».
![]()
![]()
![]()
Скорость в интервале времени ![]() – истинная мгновенная скорость
– 1‑ая производная концентрации по времени.
– истинная мгновенная скорость
– 1‑ая производная концентрации по времени.
Скорость химических реакций зависит :
1. от природы реагирующих веществ;
2. от концентрации реагентов;
3. от катализатора;
4. от температуры;
5. от степени измельчения твёрдого вещества (гетерогенные реакции);
6. от среды (растворы);
7. от формы реактора (цепные реакции);
8. от освещения (фотохимические реакции).
Основной закон химической кинетики – закон действующих масс : скорость химической реакции пропорциональна произведению концентраций реагирующих веществ в реакции
![]() :
: ![]() ,
,
где ![]() – постоянная скорости химической реакции
– постоянная скорости химической реакции
Физический смысл ![]() при
при ![]() .
.
Если в реакции участвуют не 2‑е частицы, а более ![]() , то:
, то: ![]() ~
~![]() в степенях, равных стехиометрическим коэффициентам, т.е.:
в степенях, равных стехиометрическим коэффициентам, т.е.: ![]() , где
, где
![]() – показатель порядка реакции в целом (реакции первого, второго, третьего … порядков).
– показатель порядка реакции в целом (реакции первого, второго, третьего … порядков).
Число частиц, участвующих в этом акте реакции определяет молекулярность реакции :
![]() мономолекулярная (
мономолекулярная (![]() )
)
![]() бимолекулярная (
бимолекулярная (![]() )
)
![]() тримолекулярная.
тримолекулярная.
Больше 3‑х не бывает, т.к. столкновение более 3‑х частиц сразу – маловероятно.
Когда реакция идёт в несколько стадий, то общая ![]() реакции =
реакции = ![]() наиболее медленной стадии (лимитирующей стадии).
наиболее медленной стадии (лимитирующей стадии).
Зависимость скорости реакции от температуры определяется эмпирическим правилом Вант-Гоффа
: при увеличении температуры на ![]() , скорость химической реакции увеличивается в 2 – 4 раза:
, скорость химической реакции увеличивается в 2 – 4 раза: ![]() .
.
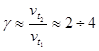
![]() ,
,
где ![]() – температурный коэффициент скорости химической реакции
– температурный коэффициент скорости химической реакции 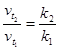 .
.
Не всякое столкновение молекул сопровождается их взаимодействием. Большинство молекул отскакивают как упругие шарики. И только активные при столкновении взаимодействуют друг с другом. Активные молекулы обладают некоторой избыточной ![]() но сравнению с неактивными молекулами, поэтому в активных молекулах связи между ними ослаблены.
но сравнению с неактивными молекулами, поэтому в активных молекулах связи между ними ослаблены.
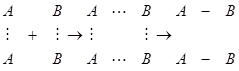
Энергия для перевода молекулы в активное состояние – энергия активации ![]() . Чем она меньше, тем больше частиц реагируют, тем больше скорость химической реакции.
. Чем она меньше, тем больше частиц реагируют, тем больше скорость химической реакции.
Величина ![]() зависит от природы реагирующих веществ. Она меньше
зависит от природы реагирующих веществ. Она меньше ![]() диссоциации – наименее прочной связи в реагентах.
диссоциации – наименее прочной связи в реагентах.
Изменение ![]() в ходе реакции:
в ходе реакции:
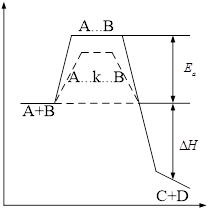
![]() выделяется (экзотермическая)
выделяется (экзотермическая)
С увеличением температуры число активных молекул растёт, поэтому ![]() увеличивается.
увеличивается.
Константа ![]() химической реакции связана с
химической реакции связана с
![]() :
: ![]() ,
,
где ![]() – предэкспоненциальный множитель (связан с вероятностью и числом столкновений).
– предэкспоненциальный множитель (связан с вероятностью и числом столкновений).
В зависимости от природы реагирующих веществ и условий их взаимодействия, в элементарных актах реакций могут принимать участие атомы, молекулы, радикалы или ионы.
Свободные радикалы чрезвычайно реакционноспособны, ![]() активных радикальных реакций очень мала (
активных радикальных реакций очень мала (![]() ).
).
Образование свободных радикалов может происходить в процессе распада веществ при температуре, освещении, под действием ядерных излучений, при электроразряде, сильных механических воздействиях.
Многие реакции протекают по цепному механизму . Особенность цепных реакций состоит в том, что один первичный акт активации приводит к превращению огромного числа молекул исходных веществ.
Например: ![]() .
.
При обычной температуре и рассеянном освещении реакция протекает крайне медленно. При нагревании смеси газов или действия света, богатого УФ лучами (прямой солнечный свет, свет от горящего ![]() ) смесь взрывается.
) смесь взрывается.
Эта реакция протекает через отдельные элементарные процессы. Прежде всего, за счёт поглощения кванта энергии УФ лучей (или температуры) молекула ![]() диссоциируется на свободные радикалы – атомы
диссоциируется на свободные радикалы – атомы ![]() :
: ![]() , затем
, затем ![]() , затем
, затем ![]() и т.д.
и т.д.
Естественно, возможно столкновение свободных радикалов и друг с другом, что приводит к обрыву цепей: ![]() .
.
Кроме температуры на реакционную способность веществ существенное влияние оказывает свет. Воздействие света (видимого, УФ) на реакции изучает раздел химии – фотохимия.
Фотохимические процессы весьма разнообразны. При фотохимическом действии молекулы реагирующих веществ, поглощая кванты света, возбуждаются, т.е. становятся реакционноспособными или распадаются на ионы и свободные радикалы. На фотохимических процессах основана фотография – воздействие света на светочувствительные материалы (фотосинтез).
Одним из наиболее распространённых в химической практике методов ускорения химических реакций является катализ
. Катализаторы
– вещества, изменяющие ![]() химической реакции за счёт участия в промежуточном химическом взаимодействии с компонентами реакции, но восстанавливающие после каждого цикла промежуточного взаимодействия свой химический состав.
химической реакции за счёт участия в промежуточном химическом взаимодействии с компонентами реакции, но восстанавливающие после каждого цикла промежуточного взаимодействия свой химический состав.
Увеличение ![]() каталитической реакции связано с меньшей
каталитической реакции связано с меньшей ![]() нового пути реакции. Т.к. в выражении для
нового пути реакции. Т.к. в выражении для ![]()
![]() входит в отрицательный показатель степени, то даже небольшое уменьшение
входит в отрицательный показатель степени, то даже небольшое уменьшение ![]() вызывает очень большое увеличение
вызывает очень большое увеличение ![]() химической реакции.
химической реакции.
Существуют 2 вида катализаторов :
гомокатализаторы;
гетерокатализаторы.
Биологические катализаторы – ферменты .
Ингибиторы
– вещества, замедляющие ![]() химической реакции.
химической реакции.
Промоторы – вещества, усиливающие действие катализаторов.
Реакции, которые протекают только в одном направлении и идут до конца – необратимые (образование осадка, выделение газа). Их мало.
Большинство реакций – обратимые
: 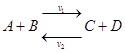 .
.
Согласно закону действия масс: ![]()
![]()
![]() – химическое равновесие
.
– химическое равновесие
.
Состояние системы, в которой ![]() прямой реакции =
прямой реакции = ![]() обратной реакции, называется химическим равновесием
.
обратной реакции, называется химическим равновесием
.
![]()
![]()
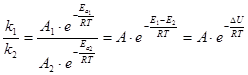 .
.
С увеличением температуры, ![]() : для эндотермической реакции возрастает, для экзотермической реакции убывает для
: для эндотермической реакции возрастает, для экзотермической реакции убывает для ![]() остаётся постоянным.
остаётся постоянным.
Влияние различных факторов на положение химического равновесия определяется принципом Ла-Шателье : если на систему, находящуюся в равновесии, оказать какое-либо воздействие, то в системе усиливаются процессы, стремящиеся уменьшить это воздействие.
В состоянии равновесия ![]() .
.
Похожие работы
-
Билеты по химии
Билеты по химии и частичные ответы на некоторые из них Билет №1 Простые вещества . Количество вещества. Число Авогадро. Качественный анализ анионов и катионов.
-
Шпоры по химии
(В)=m (В) M Ф.Е. (В)=М(В)/Z(B) Закон Авогадро Закон эквивалентов (А)/М (В)=(М(А)/z )/(M(B)/z Концентрация 1.Массовая доля w=m 2.Молярная концентрация С
-
Подразделения химии
ОГЛАВЛЕНИЕ 1) Аналитическая Химия 2) Бионеорганическая Химия 3) Биоорганическая Химия 4) Биохимия 5) Геохимия 6) Гидрохимия 7) Мезонная Химия 8) Иммуннохимия
-
Билеты для подготовки к экзамену по химии - декабрь 2000
Экзаменационный билет по предмету ХИМИЯ Билет № Какая химическая связь называется ковалентной? Приведите примеры химических соединений с ковалентной связью.
-
Кинетика окисления сплавов в атмосфере воздуха при высокой температуре
Федеральное агентство по образованию Российской Федерации Кафедра физической химии Отчет по лабораторной работе на тему: "Кинетика окисления сплавов в атмосфере воздуха при высокой температуре"
-
Электрохимия и химическая кинетика
Курсовая работа по физической химии «Электрохимия и химическая кинетика» Вариант № 9 Задача 1 Для реакции дана константа скорости омыления – К. Вычислить время, необходимое для омыления эфира, взятого в объёме V1 и концентрации С1 (н), если для омыления к указанному количеству эфира добавить:
-
Элементарное введение в химическую кинетику
Введение Основных разделов современного курса физической химии для студентов-химиков чаще всего принято выделять строение вещества, включая квантовую химию и электронную теорию химической связи - теорию валентности, химическую термодинамику и химическую кинетику.
-
Контрольная работа по Химии
Содержание 1. Задание стр. 2 2. Выполнение стр. 3 3. Список литературы стр. 9 1. ОСНОВНЫЕ ХИМИЧЕСКИЕ ПОНЯТИЯ И ЗАКОНЫ . Олово образует два оксида. Первый содержит 78,8 %, второй — 88,2% олова.
-
Эволюционная химия
ЭВОЛЮЦИОННАЯ ХИМИЯ Эволюционная химия зародилась в 1950 - 1960 гг. Под эволюционными проблемами следует понимать проблемы самопроизвольного синтеза новых химических соединений (без участия человека). Эти соединения являются более сложными и более высокоорганизованными продуктами по сравнению с исходными веществами.
-
Отчет по лабораторной работе Термодинамика
2. Теоретическая часть. Раздел химии, изучающий скорость и механизм протекания физико-химических процессов, называется химической кинетикой. Кинетика позволяет выяснить реальные механизмы протекания процессов. В химической кинетике различают гомогенные и гетерогенные процессы.