Название: Таблица по разделу Органическая химия
Вид работы: реферат
Рубрика: Химия
Размер файла: 20.95 Kb
Скачать файл: referat.me-369188.zip
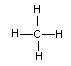
Краткое описание работы: Предельные углеводороды . Непредельные углеводороды . Ароматические или Арены Алканы Циклоалканы Алкены Диеновые Алкины 1.Общая формула CnH2n -МЕТАН
Таблица по разделу Органическая химия
| Предельные углеводороды . | Непредельные углеводороды . |
Ароматические или Арены |
||||
|
Алканы |
Циклоалканы |
Алкены |
Диеновые |
Алкины |
||
|
1.Общая формула |
CnH2n CH4-МЕТАН С6Н12-ГКСАН С10Н22-ДЕКАН |
CnH2n С6Н12-ЦИКЛОГЕКСАН С3Н6-ЦИКЛОПРОПАН С4Н8-ЦИКЛОБУТАН |
CnH2n С2Н4-ЭТЕН С6Н12-ГЕКСЕН С4Н8-БУТЕН |
CnH2N-2 С3Н8-ПЕНТАДИЕН С3Н4-ПРОПАДИЕН С6Н10-ГЕКСАДИЕН |
CnH2N-2 С3Н4-ПРОПИН С4Н6-БУТИН С7Н12-ГЕПТИН |
CnH2n-6 С6Н6-БЕНЗОЛ С7Н8-ТУЛУОЛ С8Н10-КСИЛОЛ |
|
2.Строение |
||||||
| А) тип гибридизации |
sp3 -гибридизация |
sp3 -гибридизация |
sp2-гибридизация |
sp-гибридизация |
sp-гибридизация |
sp2-гибридизация |
| Б) угол связи |
∟ 109*28' |
∟ 60*, 90*, 100*, 120* |
∟120* |
∟ 120* |
∟ 180* |
∟ 120* |
| В) длина связи (нм) |
0,154 |
0,154 |
0,134 |
0,134 |
0,12 |
0,142 |
| Г) форма молекулы |
тетраэдр |
стремится к тетраэдру |
плоская |
плоская |
линейная |
плоская |
| Д) структурная формула |
H H C H (МЕТАН) H |
CH2 CH2---------CH2 (ЦИКЛОПРОПАН) |
Н H C=C H H (ЭТЕН) |
CH2=C=CH2 (ПРОПАДИЕН 1,2) |
HC≡CH (ЭТИН) |
CH (БЕНЗОЛ) HC HC CH CH |
|
3.Изомерия |
||||||
|
1.Структурная |
По положению заместителя в ядре ! |
|||||
| А) строение углеродного скелета |
1) H3C-CH2-CH2-CH3 (Бутан) 2)H3C-CH-CH3 CH3 (2метил пропан) |
1) CH2-CH-CH3 CH2-CH2 (метил бутан) |
1) CH2=CH-CH2-CH3 (бутен 1) 2) CH2=C-CH3 CH3 (метилпрорен 1) |
1)CH2=C=CH-CH2-CH3 (пентадиен 1,2) 2)CH2=C=C-CH3 CH3 (2метилБутадиен1,2) |
1)CH≡C-CH2-CH2-CH3 (пентин 1) 2)CH≡C-CH-CH3 CH3 (2метилбутин1) |
1) CH3 2) CH3
CH3
3 CH3 |
| Б) по положению двойной (тройной) связи |
CH2=CH-CH2-CH3 (бутен 1) CH3-CH=CH-CH3 (бутен2) |
1)CH2=C=CH-CH2-CH3 (пентадиен 1,2) 2)CH3=CH-CH=CH-CH3 (пентадиен 1,3) |
1)CH≡C-CH2-CH3 (бутин 1) 2)CH3-C≡C-CH3 (бутин 2) |
|||
| В) с углеводородом Другого класса |
1)с алкенами 2) CH CH2=CH-CH3 CH--------CH (пропен) (циклопропан) |
С циклоалканами (см циклоалканы) | С алкинами (см Алкины) |
С диеновыми : 1) CH2=C=CH2 (пропадиен) 2) CH≡C-CH3 (пропин) |
||
| Г) по положению радикала |
1) CH2-CH-CH3 2)CH2-CH-CH3 CH2-CH-CH3 CH3-CH-CH2 (1,2диметилбутан) (1,3диметилбутан) |
|||||
|
2.Пространственная |
||||||
| Д)Пространственная изомерия (цис-транс изомерия) |
CH3 CH3 CH3 H C=C C=C H (цис) H H (транс) CH3 |
CH3 CH=CH2 CH3 H C=C C=C H H H CH=CH2 |
||||
|
3.Химические свойства . |
||||||
| А)Горение |
CH4+O2→CO2+H2O+Q МЕТАН |
CH2 CH2-----CH2+O2→CO2+H2O+Q |
С2H4+O2→CO2+H2O+Q ЭТЕН |
Те же свойства что и у алкенов но реакции происходят в 2 этапа ! |
1.полное сгорание 2C2H2+5O2→4CO2+2H2O+Q 2 неполное сгорание С2H2+O2→C+H2O |
1.полное сгорание C6H6 +O2→CO2+H2O 2. Неполное сгорание C6H6+O2→C+H2O+Q |
| Б)Термическое разложение |
C4H10→4C+5H2+Q БУТАН |
С2H4→C+H2-Q ЭТЕН |
1. CH2=CH-CH=CH2+H2→ бутадиен CH2-CH=CH-CH2 Бутен2 H H 2. CH3-CH=CH=CH3+H2→ бутэн2 CH3-(CH2)2-CH3 бутан |
C2H2→C+H2 |
C6H6→C+H2-Q |
|
| В)р замещения |
*CH4+CL2→CH3CL+HCL хлорметан *CH3CL+CL2→CH2CL2+HCL дихлорметан *CH2CL2+CL=CHCL3+HCL Трихлорметан *CHCL3+CL2→CCL4+HCL тэтрахлорметан |
C7H14+Br2→C7H13Br+HBr (бромциклогептан) |
1. C6H6+CL2→C6H5-CL хлорбензол 2.C6H6+HNO3→C6H5-NO3 нитробензол |
|||
|
Г)Р присоединения (+H2, +H HAL ,+HAL2, +H2O) |
Р изомеризации CH3-CH2-CH2-CH3→ CH3-CH-CH3 CH3 (2 МЕТИЛПРОПАН) |
CH CH2—CH2+H2→CH3-CH2-CH3 (пропан) СH2 CH2---CH2+Br2→CH2+CH2+CH2 (1,3ДИБРОМПРОПАН) Br Br |
*CH2=CH2+H2→CH3+CH3 ЭТАН *С2H4+HOH→CH3-CH2OH ЭТАНОЛ *C2H4+HCL→CH3-CH2CL ХЛОРЭТАН *C2H4+CL2→CH2CL-CH2CL ДИХЛОРЭТАН |
2 ЭТАПА : ≡→=→- 1. CH≡CH+2H2→CH3-CH3 ЭТИН 2. СH≡CH+2CL2→ ЭТИН CHCL2-CHCL2 (1122ТЕТРАХЛОЭТАН) 3. C2H2+2HCL→CH2CL=CH2CL 1,2 ДИХЛОРЭТАН 4. C2H2+H2O→CH3-C=O H (Альдегид) |
1. Гидрирование C6H6+3H2→C6H12 (циклогексан) 2.C6H6+3CL2→C6H5CL |
|
| Д) Полимеризация |
*2С2H4+O2→2CH2-CH2 O ПОЛИЭТИЛЕН |
n(CH2=CH-CH=CH2) → ДИВИНИЛ (-CH2-CH=CH-CH2-)n поливинил |
3C2H2→C6H6 (Бензол) |
|||
|
Предельные у-в. |
Непредельные у-в. |
Ароматические |
|||||
|
Алканы |
Циклоалканы |
Алкены |
Алкодиены |
Алкины |
Арены |
||
|
I |
Общая формула |
CnH2n |
CnH2n |
CnH2n |
CnH2n-2 |
CnH2n-3 |
CnH2n-6 |
|
1 |
|||||||
|
Тип гибридизации |
Sp3 |
Sp3 |
Sp2 |
Sp2 |
Sp |
Sp2 |
|
|
2 |
|||||||
|
Угол связи |
109*28' |
Разный |
120* |
120* |
180* |
120* |
|
|
3 |
|||||||
|
Длина связи (нм) |
0,154 |
0,154 |
0,134 |
0,134 |
0,12 |
0,14 |
|
|
4 |
|||||||
|
Форма молекулы |
Тэтрайдр |
Стремится к тэтрайдеру |
Плоская |
Плоская |
Линейная |
Плоская |
|
|
5 |
|||||||
|
Структурная формула |
|
|
|||||
|
6 |
|||||||
|
Изомерия |
|||||||
|
II |
|||||||
|
Структурная |
Структурная |
Структурная |
Структурная |
Структурная |
Структурная |
Структурная |
|
|
А |
|||||||
|
По строению скелета |
А |
А |
А Б В(С циклоалканами) |
А Б В(С алкенами) |
А Б В(С алкодиенами) |
А |
|
|
Б |
|||||||
|
По положению P связи |
В |
ДПространственная измерия (Цис-трансизомерия) |
ДПространственная измерия (Цис-трансизомерия) |
_____________ |
|||
|
В |
|||||||
|
С углеводородами другово класса . |
|||||||
|
Г |
|||||||
|
Пространственная измерия |
|||||||
|
Д |
|||||||
Похожие работы
-
Алканы
Алканы - это предельные углеводороды, в молекулах которых все атомы связаны одинарными связями. Формула - Физические свойства Температуры плавления и кипения увеличиваются с молекулярной массой и длиной главной углеродной цепи
-
Характеристика углеводородов
ДИЕНОВЫЕ УГЛЕВОДОРОДЫ (АЛКАДИЕНЫ) Диеновые углеводороды или алкадиены – это непредельные углеводороды, содержащие две двойные углерод - углеродные связи. Общая формула алкадиенов CnH2n-2.
-
Углеводороды (таблица)
Предельные углеводороды . Непредельные углеводороды . Ароматические или Арены Алканы Циклоалканы Алкены Диеновые Алкины 1.Общая формула CnH2n -МЕТАН
-
Химия (Шпаргалка)
Метан C2 H6 Этан C3 H8 Пропан C4 H10 Бутан C5 H12 Пентан C6 H14 Гексан C7 H16 Гептан C8 H18 Октан C9 H20 Нонан C10 H22 Декан 1.Все атомы, образ. молекулы орган. вещ-в, связаны в опред. послед. согласно их валентностям.
-
Химия
Вопросы Гомологические ряды Алканы Алкены Алкины Общее понятие Общая формула 2n+2 2n-2 Тип гибридизации Число сигма связей 4.Наличие других видов связи
-
Получение алканов, алкенов, алкинов. Важнейшие представители. Применение в промышленности
Министерство образования Р.Ф. Курская государственная сельскохозяйственная академия им. Проф. И. И. Иванова РЕФЕРАТ ПО Органической химии ТЕМА: ПОЛУЧЕНИЕ АЛКАНОВ,АЛКЕНОВ,АЛКИНОВ.
-
Органические соединения
Реферат 61314.0.1287405047.doc по химии Оглавление. Предельные углеводороды. (Алканы.). Нонан. 2 Непредельные углеводороды (Алкены. Алкины). Нонен-1. 4
-
Нефть
Реферат на тему “Нефть”. Нефть -масляная горючая жидкость обычно темного цвета со своеобразным запахом она немного легче воды и в ней не растворяется.
-
Предельные углеводороды
Алканы - предельные углеводороды, содержащие только простые связи углерода. Получение алканов: промышленный метод, нитрование и окисление. Углеводороды, содержащие двойную связь углерода - алкены или этиленовые углеводороды. Диеновые углеводороды.
-
Характеристика ацетиленовых углеводородов
АЦЕТИЛЕНОВЫЕ УГЛЕВОДОРОДЫ (АЛКИНЫ) Ацетиленовыми углеводородами (алкинами) называются непредельные (ненасыщенные) углеводороды, содержащие в молекуле одну тройную связь и имеющие общую формулу CnH2n-2. Родоначальником гомологического ряда этих углеводородов является ацетилен HCCH.