Название: Окислительно-восстановительные реакции 2
Вид работы: реферат
Рубрика: Химия
Размер файла: 368.17 Kb
Скачать файл: referat.me-370234.docx
Краткое описание работы: Окислительно-восстановительные реакции Вводная часть Учитель. В III в. до н.э. на острове Родос был построен памятник в виде огромной статуи Гелиоса (у греков – бог Солнца). Грандиозный замысел и совершенство исполнения Колосса Родосского – одного из чудес света – поражали всех, кто его видел.
Окислительно-восстановительные реакции 2
Окислительно-восстановительные реакции
Вводная часть
Учитель. В III в. до н.э. на острове Родос был построен памятник в виде огромной статуи Гелиоса (у греков – бог Солнца). Грандиозный замысел и совершенство исполнения Колосса Родосского – одного из чудес света – поражали всех, кто его видел.
Мы не знаем точно, как выглядела статуя, но известно, что она была сделана из бронзы и достигала в высоту около 33 м. Статуя была создана скульптором Харетом, на ее строительство ушло 12 лет.
Бронзовая оболочка крепилась к железному каркасу. Полую статую начали строить снизу и, по мере того как она росла, заполняли камнями, чтобы сделать ее устойчивее. Примерно через 50 лет после завершения строительства Колосс рухнул. Во время землетрясения он переломился на уровне колен.
Ученые считают, что истинной причиной недолговечности этого чуда стала коррозия металла. А в основе процесса коррозии лежат окислительно-восстановительные реакции.
Сегодня на уроке вы познакомитесь с окислительно-восстановительными реакциями; узнаете о понятиях «восстановитель» и «окислитель», о процессах восстановления и окисления; научитесь расставлять коэффициенты в уравнениях окислительно-восстановительных реакций. Запишите в своих рабочих тетрадях число, тему урока.
Изучение нового материала
Учитель. Запишите молекулярные уравнения следующих реакций: взаимодействие сульфата меди (II) со щелочью и взаимодействие этой же соли с железом.
В каждом уравнении расставьте степени окисления элементов в формулах исходных веществ и продуктов реакции.
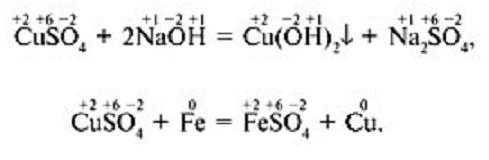
Учитель. Изменились ли степени окисления элементов в этих реакциях?
Ученик. В первом уравнении степени окисления элементов не изменились, а во втором изменились – у меди и железа.
Учитель. Вторая реакция относится к окислительно-восстановительным. Попробуйте дать определение окислительно-восстановительных реакций.
Ученик. Реакции, в результате которых изменяются степени окисления элементов, входящих в состав реагирующих веществ и продуктов реакции, называют окислительно-восстановительными реакциями.
Учащиеся записывают в тетради под диктовку учителя определение окислительно-восстановительных реакций.
Учитель. Что же произошло в результате окислительно-восстановительной реакции? До реакции у железа была степень окисления 0, после реакции стала +2. Как видим, степень окисления повысилась, следовательно, железо отдает 2 электрона.
У меди до реакции степень окисления +2, после реакции – 0. Как видим, степень окисления понизилась. Следовательно, медь принимает 2 электрона.
Железо отдает электроны, оно является восстановителем, а процесс передачи электронов называется окислением.
Медь принимает электроны, она – окислитель, а процесс присоединения электронов называется восстановлением.
Запишем схемы этих процессов:

Итак, дайте определение понятий «восстановитель» и «окислитель».
Ученик. Атомы, молекулы или ионы, которые отдают электроны, называют восстановителями.
Атомы, молекулы или ионы, которые присоединяют электроны, называют окислителями.
Учитель. Какое определение можно дать процессам восстановления и окисления?
Ученик. Восстановлением называют процесс присоединения электронов атомом, молекулой или ионом.
Окислением называют процесс передачи электронов атомом, молекулой или ионом.
Учащиеся записывают под диктовку определения в тетрадь и выполняют рисунок.
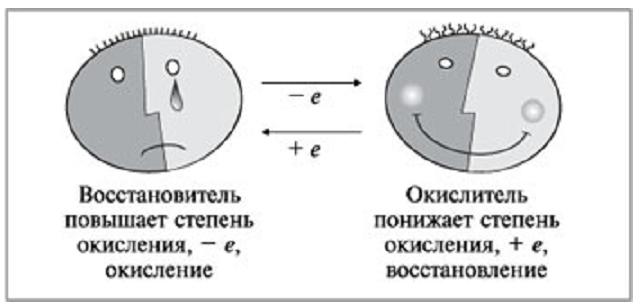
Запомните!
Отдать электроны – окислиться.
Взять электроны – восстановиться.
Учитель. Окисление всегда сопровождается восстановлением, и наоборот, восстановление всегда связано с окислением. Число электронов, отдаваемых восстановителем, равно числу электронов, присоединяемых окислителем.
Для подбора коэффициентов в уравнениях окислительно-восстановительных реакций используют два метода – электронного баланса и электронно-ионного баланса (метод полуреакций).
Мы рассмотрим только метод электронного баланса. Для этого используем алгоритм расстановки коэффициентов методом электронного баланса.

П р и м е р. Расставьте коэффициенты в данной схеме реакции методом электронного баланса, определите окислитель и восстановитель, укажите процессы окисления и восстановления:
Fe2O3 + CO → Fe + CO2.
Решение
Воспользуемся алгоритмом расстановки коэффициентов методом электронного баланса.


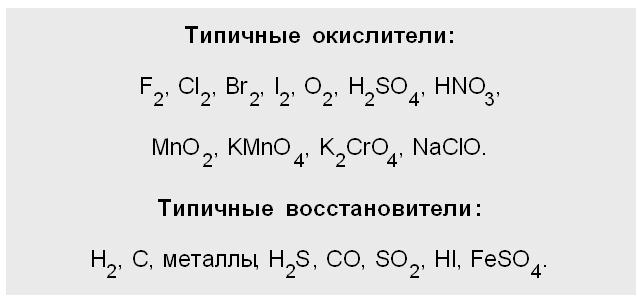
Учитель. Окислительно-восстановительные реакции очень распространены. С ними связаны не только процессы коррозии, но и брожение, гниение, фотосинтез, процессы обмена веществ, протекающие в живом организме. Их можно наблюдать при сгорании топлива. Окислительно-восстановительные процессы сопровождают круговороты веществ в природе.
Заключительная часть
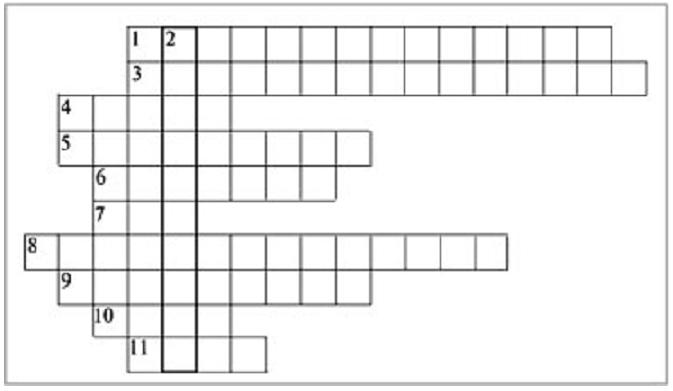
Учитель предлагает учащимся разгадать кроссворд по изученному материалу. Результат работы сдается на проверку.
Разгадав кроссворд, вы узнаете, что вещества КМnО4, К2Сr2O7, О3 – cильные … (по вертикали (2)).


Похожие работы
-
Окислительно-восстановительный реакции
Окисли?тельно-восстанови?тельные реа?кции (ОВР) — это встречно-параллельные химические реакции, протекающие с изменением степеней окисления атомов, входящих в состав реагирующих веществ, реализующихся путём перераспределения электронов между атомом-окислителем и атомом-восстановителем.
-
История одного металла Медь и ее сплавы
История одного металла. Медь и её сплавы. Введение. Золотая маска фараона Тутанхамона. Золотой самородок «Мефистофель» массой 20,25 г, найденный Сибири. Алмазный фонд. Москва.
-
Билеты по химии
Билеты по химии и частичные ответы на некоторые из них Билет №1 Простые вещества . Количество вещества. Число Авогадро. Качественный анализ анионов и катионов.
-
Пероксид водрода
Химические свойства Перокси́д водоро́да перекись водорода — простейший представитель пероксидов. Бесцветная жидкость с «металлическим» вкусом, неограниченно растворимая в воде, спирте и эфире. Концентрированные водные растворы взрывоопасны. Пероксид водорода является хорошим растворителем.
-
Классификация химических реакций 3
Лекция 2. Химические реакции. Классификация химических реакций. Окислительно-восстановительные реакции Вещества, взаимодействуя друг с другом подвергаются различным изменениям и превращениям. Например, уголь, сгорая образует углекислый газ. Бериллий, взаимодействуя с кислородом воздуха превращается в оксид бериллия.
-
Элементы d-блока периодической системы
Химические свойства элементов d-блока периодической системы, их содержание и биологическая роль в организме. Рассмотрение кислотно-основных и окислительно-восстановительных реакций 3d-элементов. Механизмы действия карбоангидраза и алькогольдегидрогеназа.
-
Классификация химических реакций
Общее понятие о химической реакции, ее сущность, признаки и условия проведения. Структура химических уравнений, их особенности и отличия от математических уравнений. Классификация и виды химических реакций: соединения, разложения, обмена, замещения.
-
Химические реакции
Содержание. стр. 1. Химические реакции. 2. Окислительно-восстановительные реакции. 3. Реакции в растворах электролитов. 4. Представление о кислотах и основаниях.
-
Понятие химических реакций и их классификация
Химическая реакция как превращение вещества, сопровождающееся изменением его состава и (или) строения. Признаки химических реакций и условия их протекания. Классификация химических реакций по различным признакам и формы их записи в виде уравнений.
-
Контрольная работа по Химии
Содержание 1. Задание стр. 2 2. Выполнение стр. 3 3. Список литературы стр. 9 1. ОСНОВНЫЕ ХИМИЧЕСКИЕ ПОНЯТИЯ И ЗАКОНЫ . Олово образует два оксида. Первый содержит 78,8 %, второй — 88,2% олова.