Название: Мембранное равновесие Доннана (Доклад)
Вид работы: реферат
Рубрика: Химия
Размер файла: 20.78 Kb
Скачать файл: referat.me-369035.docx
Краткое описание работы: Мембранное равновесие, связанное с различием концентрации солей внутри и вне клеток, известно давно. В 1911 г. Ф. Доннан объяснил это явление, впоследствии названное его именем.
Мембранное равновесие Доннана (Доклад)
Мембранное равновесие, связанное с различием концентрации солей внутри и вне клеток, известно давно. В 1911 г. Ф. Доннан объяснил это явление, впоследствии названное его именем.
Мембранное равновесие Доннана связано с переносом некоторого количества вещества низкомолекулярного электролита внутрь пространства, содержащего полимер, и, вследствие этого, неравномерного распределения концентраций этого электролита по обе стороны полупроницаемой мембраны.
Пусть в некоторый начальный момент времени концентрации ионов низкомолекулярного и высокомолекулярного соединений по обе стороны мембраны распределяются следующим образом:
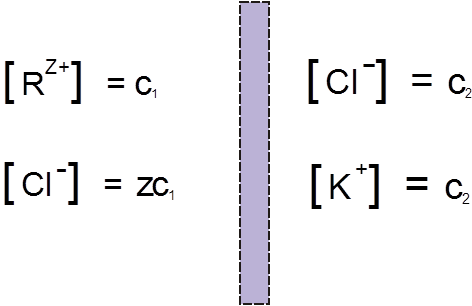 |
Рис 1.
В левой части сосуда, разделенного полупроницаемой мембраной, находится раствор полимера, который в результате диссоциации представлен поликатионом R(Z+) и противоионом Cl– , концентрации которых равны соответственно C1 и ZC1 . В левой части – раствор низкомолекулярного электролита, например KCl, с концентрацией С2 , диссоциирующий на К+ и Cl– . При установлении равновесия вследствие диффузии в такой системе малые ионы K+ перемещаются преимущественно из правой части сосуда в левую. Макрокатионы R(Z+) не могут проникать через мембрану, поэтому для сохранения электронейтральности вместе с катионами K+ справа налево происходит перемещение избыточного числа анионов Cl– . В результате этих процессов концентрация низкомолекулярного электролита в растворе ВМС повышается:
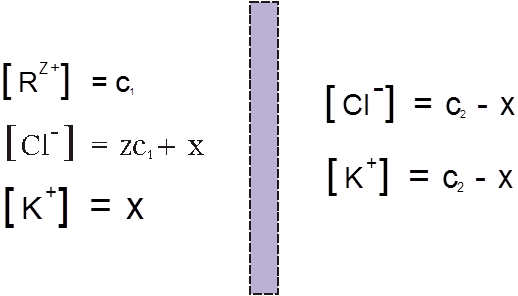 |
Рис 2.
Условием равновесия является равенство произведений концентраций электролитов в левой и правой части сосуда, разделенного полупроницаемой мембраной:
[K+ ]внутр. [Cl– ]внутр. = [K+ ]внеш. [Cl– ]внеш.
Подставляя обозначения из рис.2, имеем уравнение:
X (ZC1 + X) = (C2 – X)2
Решая это уравнение относительно X, получаем:
C2 2
![]() X = .
X = .
ZC1 + 2C2
Это и есть уравнение Доннана, которое показывает количество низкомолекулярного вещества, переносимого в фазу ВМС через полупроницаемую мембрану. Из него следует вывод, что низкомолекулярный электролит распределяется неравномерно по обе стороны мембраны. Перенос вещества всегда существует из внешнего раствора во внутренний, в результате чего во внутреннем растворе наблюдается более высокая концентрация переносимых электролитов по сравнению с внешним раствором. Этим же объясняется некоторый избыток осмотического давления в растворах, содержащих ВМС и электролиты.
Если концентрация низкомолекулярного электролита намного больше концентрации полимера (С2 >> C1 ), то X = C2 /2 , т.е. при малых концентрациях макроионов и больших концентрациях малых ионов наблюдается равномерное распределение малых ионов по обе стороны мембраны.
При обратном соотношении концентраций (C2 << C1 ), XZC1 = C2 2 , откуда следует, что перенос X очень мал и обратно пропорционален величине ZC1 .
Осмотическое давление раствора в левом отсеке складывается из осмотического давления, обусловленного присутствием ВМС и низкомолекулярного соединения:
p 1 = p 1 (ВМС) + p 1 (НМС) – p 2 (НМС).
Та часть осмотического давления крови, которая создается растворенными в ней белками, называется онкотическим давлением. Хотя по абсолютной величине оно, как правило, незначительно (например, для плазмы крови на долю осмотического давления, создаваемого растворами белков приходится всего лишь 0,5 – 1 %), эта составляющаяимеет большое физиологическое значение.
Все биологические мембраны полупроницаемы: в нормальных условиях проницаемы для неорганических солей и воды и непроницаемы для белков и полисахаридов. Этот эффект является одной из причин неравномерного распределения ионов вне и внутри клетки.
Похожие работы
-
Регуляция в системе органов пищеварения
Процессы жизнедеятельности в организме, связанные с расходом энергии и разрушением клеток тканей, требуют постоянного пополнения энергетического и пластического материала. Усвоению пищевых веществ предшествует сложная обработка их в результате процессов пищеварения, представляющих собой начальный этап обмена веществ.
-
Билеты по химии
Билеты по химии и частичные ответы на некоторые из них Билет №1 Простые вещества . Количество вещества. Число Авогадро. Качественный анализ анионов и катионов.
-
Витамины 10
Министерство образования и науки Челябинской области ГОУ СПО (ССУЗ) Катав-Ивановский индустриальный техникум Специальность 230103 Доклад По дисциплине: «Химия»
-
Термодинамические характеристики (H,S,G) и возможность самопроизвольного протекания процесса
Уравнение химической реакции с использованием электронно-ионного метода. Определение потенциалов окислителя и восстановителя, направления протекания процесса, термодинамических характеристик H,S,G. Электронная формула элементов по 2 и 4 квантовым числам.
-
Шпоры по химии
(В)=m (В) M Ф.Е. (В)=М(В)/Z(B) Закон Авогадро Закон эквивалентов (А)/М (В)=(М(А)/z )/(M(B)/z Концентрация 1.Массовая доля w=m 2.Молярная концентрация С
-
Древняя история нефти
Доклад по химии. Древняя история нефти. Ученицы 10 "б" класса средней школы N45 Хорьяковой Людмилы 2001год. В наши дни нефть является важнейшим химическим сырьем и энергетическим источником. В 1962 году ее мировая добыча составила 1.1 миллиарда тонн. Каждый год открывают все новые нефтяные месторождения.
-
Свойства, применение и получение полиметилметакрилата
Доклад по химии на тему : «Свойства, применение, получение полиметилметакрилата Выполнил: Елизарьев Леонид Школа № 43, 11 класс «Б». Полиметилметакрилат.
-
Полиметилметакрилат. Органическое стекло
Доклад по органической химии ученика 11”А” класса гимназии N1542 Макаровского Александра по теме: “Полиметилметакрилат. Органическое стекло”
-
Крахмал (Доклад)
Министерство Образования Российской Федерации Доклад по Химии на тему Крахмал Выполнил: Ученик 10 кл. Б Нечин Евгений Красноярск, 1998 Крахмал Крахмал состоит из 2 полисахаридов - амилозы и амилопектина, образованных остатками глюкозы. Экспериментально доказано, что химическая формула крахмала (C6H10O5)n.
-
Серебро 2
Доклад По химии на тему: «Однородные вещества» Выполнила: Ученица 7ª классаМОУСОШ № 42Кокшарова Татьяна. Копейск 2007 год. Серебро. Серебро (от лат. Argentum), химический элемент; металл белого цвета, пластичный, хорошо полируется. В природе находится в виде двух стабильных изотопов 107Ag и 109Ag; из радиоактивных изотопов практически важен 110Ag.